Processi isotermi. Trasformatore ideale di energia
Gennaio 10th, 2022 | by Marcello Colozzo |
Ci proponiamo di determinare la quantità Q > 0 di calore assorbita da un sistema termodinamico che compie lavoro sull'ambiente (L > 0). Al solito e senza perdita di generalità, consideriamo il lavoro meccanico eseguito dalle forze di pressione, per cui il primo principio si scrive:

Poiché le variabili indipendenti sono T,V il differenziale totale dell'energia interna si scrive:

Se il processo è isotermo i.e. avviene a temperatura costante:

Ne segue

Questa equazione ci dice che in una espansione isoterma elementare (dV > 0), la quantità dQ di calore assorbita differisce dal lavoro eseguito sull'ambiente (dal sistema) per un termine proporzionale alla variazione di energia interna. Tuttavia, esiste una classe di sistemi termodinamici che conservano l'energia interna in ogni espansione isoterma reversibile, per cui dQ=dL cioè la quantità di calore assorbita dall'ambiente è completamente trasformata in lavoro sull'ambiente. Questi sistemi sono i gas perfetti, che si comportano come trasformatori ideali di energia.


 Congettura di Riemann
Congettura di Riemann Trasformata discreta di Fourier
Trasformata discreta di Fourier
 Trasformata di Fourier nel senso delle distribuzioni
Trasformata di Fourier nel senso delle distribuzioni Trasformata di Fourier
Trasformata di Fourier  Infinitesimi ed infiniti
Infinitesimi ed infiniti Limiti notevoli
Limiti notevoli Punti di discontinuità
Punti di discontinuità Misura di Peano Jordan
Misura di Peano Jordan Eserciziario sugli integrali
Eserciziario sugli integrali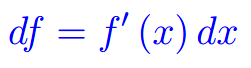 Differenziabilità
Differenziabilità 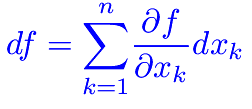 Differenziabilità (2)
Differenziabilità (2)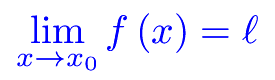 Esercizi sui limiti
Esercizi sui limiti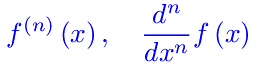 Appunti sulle derivate
Appunti sulle derivate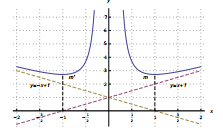 Studio della funzione
Studio della funzione Esercizi sugli integrali indefiniti
Esercizi sugli integrali indefiniti Algebra lineare
Algebra lineare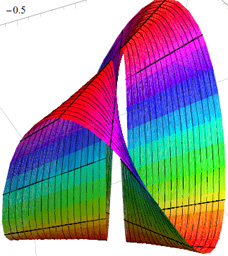 Analisi Matematica 2
Analisi Matematica 2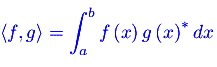 Analisi funzionale
Analisi funzionale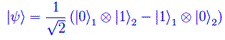 Entanglement quantistico
Entanglement quantistico Spazio complesso
Spazio complesso Biliardo di Novikov
Biliardo di Novikov Intro alla Meccanica quantistica
Intro alla Meccanica quantistica Entanglement Quantistico
Entanglement Quantistico